
In vederea conducerii in sensul dorit a operatiilor de elaborare (topire, supraincalzire, dezoxidare, degazare, rafinare, modificare) a aliajelor neferoase este necesar sa se cunoasca principalele procese fizico-chimice care au loc in perioada de elaborare.
In mare,acestea sunt urmatoarele:
- procese fizice care au loc la topirea si supraincalzirea metalelor si aliajelor;
- reactia aialejor topite cu oxigenul;
- reactia aliajelor topite cu hidrogenul si alte gaze;
- reactia aliajelor topite cu fondantii,zgura si cu captuseala cuptoarelor.
La topirea si supraincalzirea in stare lichida a metalelor si a aliajelor neferoase au loc unele procese care sunt cantitativ deosebite de acelea care se petrec la aliajele feroase.
Principalele procese sunt urmatoarele:
- topirea,de care este legata caldura necesara pentru topire;
- supraincalzirea la topire si supraincalzirea locala;
- evaporarea elementelor.
Temperatura de topire a aliajelor neferoase este foarte variata in comparatie cu cea a aliajelor feroase. Din acest punct de vedere metalele se pot imparti in urmatoarele grupe(valorile temperaturilor de topire sunt rotunjite):
- metale usor fuzibile,cu temperatura de topire sub 500![]() C (Pb -327
C (Pb -327![]() C; Sn-232
C; Sn-232![]() C;Zn-420
C;Zn-420![]() C);
C);
- metale cu temperatura medie de topire,pana la 1000![]() C (Al-660
C (Al-660![]() C; Mg-650
C; Mg-650![]() C);
C);
- metale cu temperatura ridicata de topire,pana la 1600![]() C ( Cu-1083
C ( Cu-1083![]() C; Ni-1455
C; Ni-1455![]() C; Fe-1539
C; Fe-1539![]() C; Mn -1260
C; Mn -1260![]() C; Be-1280
C; Be-1280![]() C);
C);
- metale greu fuzibile cu temperatura de topire mai mare
de 1600![]() C (Ti-1725
C (Ti-1725![]() C; Cr-1845
C; Cr-1845![]() C; Mo-2622
C; Mo-2622![]() C; W-3400
C; W-3400![]() C).
C).
Caldura necesara topirii aliajelor neferoase variaza de asemenea de la aliaj la aliaj.
Se stie ca ea se compune din caldura de incalzire de la temperatura ambianta pana la temperatura de topire, din caldura latenta de topire si din caldura de supraincalzire de la temperatura de topire si pana la temperatura de turnare:
Q = C![]() G(t
G(t![]() -t
-t![]() )+GL
)+GL![]() +C'
+C'![]() G (t
G (t![]() -t
-t![]() )
)
unde: Q este continutul de caldura al aliajului, in kcal;
C![]() , ,C'
, ,C'![]() - caldura specifica a aliajului in stare solida si lichida,
in kcal/kg
- caldura specifica a aliajului in stare solida si lichida,
in kcal/kg![]() C;
C;
G - greutatea aliajului evacuat in oala, in kg;
t![]() ,t
,t![]() , t
, t![]() -temperatura initiala,de topire si de turnare,in
-temperatura initiala,de topire si de turnare,in ![]() C;
C;
L![]() - caldura latenta de topire, in kcal/kg.
- caldura latenta de topire, in kcal/kg.
Spre deosebire de aliajele feroase, caldura necesara pentru topirea si suprancalzirea aliajelor neferoase este foarte diferita, aceasta datorita variatiei temperaturii de turnare, a caldurii specifice si a caldurii latent de topire ale metalelor de baza (tabelul 1)
Caracteristicile fizice principale ale unor metale care stau la baza aliajelor neferoase
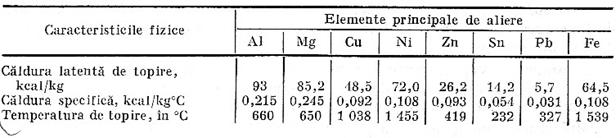
Cu cat este mai mare caldura specifica si caldura latent de topire, cu atat consumul de caldura pentru topire si supraincalzire este mai mare.
Cu cat caldura specifica a metalului si aliajului in stare lichida este mai mare, cu atat ele se vor raci mai incet in timpul umplerii formelor si cu atat mai mica trebuie sa fie suprancalzirea necesara pentru turnare.
Cu cat este mai mare caldura specifica si caldura latenta de topire a aliajului, cu atat este mai mare variatia (gradientul) de temperatura pe sectiunea piesei turnate si deci tendinta de formare a retasurii concentrate, ceea ce impune o alimentare mai puternica a acesteia (folosirea maselotelor cu dimensiuni mai mari).
Diferentele mari constante la valorile t![]() , C
, C![]() si L
si L![]() conduc la urmatoarele consecinte practice:
conduc la urmatoarele consecinte practice:
- pentru topirea si supraincalzirea cuprului pana la 1100
![]() C este necesara aproape de doua ori mai putina caldura decat
pentru topirea si supraincalzirea aceleiasi cantitati de aluminiu pana la 700
C este necesara aproape de doua ori mai putina caldura decat
pentru topirea si supraincalzirea aceleiasi cantitati de aluminiu pana la 700 ![]() C;
C;
- pentru topirea unor cantitai egale de aluminiu si de fonta se consuma aproape aceeasi cantitate de caldura, desi aluminiul se topeste la o temperature mai josa decat fonta;
- viteza de racire a aliajelor de magneziu este mult mai
mare decat cea a aliajelor de aluminiu, incat la magneziu C![]() =0,139 kcal/kg
=0,139 kcal/kg ![]() C iar la Al C
C iar la Al C![]() =0,308 kcal/kg
=0,308 kcal/kg ![]() C (deci aproape de trei ori mai mare) la o temperature de
topire aproximativ egala (Al -658
C (deci aproape de trei ori mai mare) la o temperature de
topire aproximativ egala (Al -658 ![]() C, Mg - 651
C, Mg - 651![]() C );
C );
- durata de mentinere a aliajelor de magneziu in forme metalice poate fi cu 20.30% mai mica decat cea a aliajelor de aluminiu,ceeea ce conduce la marirea productivitatii masinilor de turnare sub presiune;
- un aliaj de aluminiu (C![]() = 0,3 kcal/kg
= 0,3 kcal/kg ![]() C si t
C si t![]() =700
=700 ![]() C) va putea sta mai mult in oala, fara sa se raceasca
apreciabil, decat un aliaj de nichel (C
C) va putea sta mai mult in oala, fara sa se raceasca
apreciabil, decat un aliaj de nichel (C![]() =0,161 si t
=0,161 si t![]() =1 550.1 600
=1 550.1 600![]() C) sau un aliaj feros sau de plumb. Ultimele aliaje trebuie
turnate imediat dupa evacuarea din cuptor, deoarece pierd repede temperatura,
in timp ce un aliaj de aluminiu sau de magneziu pierde temperature foarte incet
si poate stationa in oala zeci de minute inainte de turnare.
C) sau un aliaj feros sau de plumb. Ultimele aliaje trebuie
turnate imediat dupa evacuarea din cuptor, deoarece pierd repede temperatura,
in timp ce un aliaj de aluminiu sau de magneziu pierde temperature foarte incet
si poate stationa in oala zeci de minute inainte de turnare.
Supraincalzirea aliajelor in stare lichida peste limita strict necesara dictata de conditiile turnarii trebuie evitata din cauza neajunsurilor ce o insotesc: pierderi mari de metal prin oxidare si evaporare excesiva, absorbtie mare de gaze, consum inutil de energie termica etc.
Evitarea supraincalzirii este o regula de baza la
elaborarea aliajelor neferoase. De obicei, supraincalzirea la elaborare nu
depaseste 100.200 ![]() C.
C.
Procesul de evaporare a metalelor lichide (pierderile prin evaporare) depinde de tensiunea vaporilor. Cu cat este mai mare tensiunea vaporilor cu atat pierderile sunt mai mari.
Presiunea de vapori creste cu temperatura dupa legea lui Clausius - Clapeyron si cand tensiunea vaporilor devine egala cu cea exterioara incepe fierberea metalului,adica evaoprarea in intreg volumul.
Majoritatea metalelor si aliajelor industriale au temperaturi ridicate de fierbere. Totusi unele metale (ca de ex. Cd,Zn,Mg) ating presiunea de vapori 760mm Hg, adica fierb la o temperature joasa, apropiata de temperaturile de elaborare a aliajelor metalelor neferoase intalnite in mod curent (fig. 1).
Astfel temperatura de topire si fierbere a acestor metale este :
Cd - t![]() = 321
= 321 ![]() C; t
C; t![]() =769
=769 ![]() C; Mg - t
C; Mg - t![]() = 651
= 651![]() C; t
C; t![]() =1 103
=1 103 ![]() C; Zn - t
C; Zn - t![]() =419
=419 ![]() C; tv= 907
C; tv= 907 ![]() C.
C.
In cazul aliajelor, tensiunea de vapori a unui component este proportional cu tensiunea de vapori a componentului pur si cu concentratia exprimata in fractiuni de unitati. Tensiunea de vapori a unui component din aliaj este deci mai mica decat tensiunea componentului pur.
In figura 1, b se arata ca exemplu variatia temperaturii vaporilor de zinc din aliajul Al - Zn, iar in figura 1, c - tensiunea de vapori a magneziului in aliajele Al - Mg.
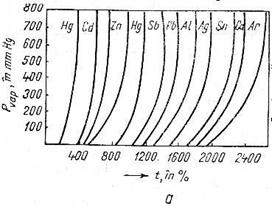
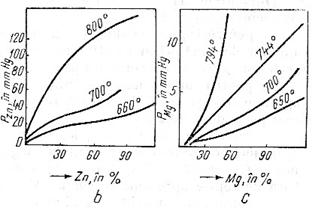
Fig. 1 Variatia tensiunii de vapoi a diferitelor metale (a) a aliajelor Al-Zn (b) si Al-Mg (c) in functie de temperatura si concentratie
Evaporarea are loc la orice temperatura, deci si in stare solida. De ex. la introducerea cuprului in cuptorul de topire , flacara se coloreaza in verde, ceea ce indica prezenta vaporilor de cupru.
Diferenta consta numai in intensitatea evaporarii. Curbele tensiunii de vapori sunt continui in intreg domeniul de temperatura (fig. 1, a).
Trecerea in stare lichida nu modifica aliura curbelor.
La topire se evaporeaza toti componentii aliajului,insa in proportii diferite. Prin evaporare se schimba compozitia aliajului, imbogatindu-se in componentii cu tensiune mica a vaporilor. De acest lucru se tine seama la calculul incarcaturii, compensand prin adaos suplimentar pierderile prin evaporare. De ex. la topirea aliajelor de aluminiu continutul de sodiu si magneziu se micsoreaza.
Pierderile prin evaporare impreuna cu pierderile prin oxidare si prin antrenarea de metal in zgura constituie pierderile de topire.
Evaporarea si pierderile prin evaporare depind, in afara de tensiunea vaporilor, deci de natura si concentratia metalului si de temperatura, inca de urmatorii factori:
- suprafata baii (pierderile sunt mai mari in cuptorul cu vatra decat in cele cu creuzet). Din acest motiv aliajele care se evapora usor se recomanda sa fie topite astfel, incat baia sa aiba suprafata cat mai mica ,iar gradul de supraincalzire in stare lichida sa fie cat mai mic;
- atmosfera cuptorului; in atomsfera reducatoare este mai intensa, in cea oxidanta este franta de pelicula de oxizi care se formeaza la suprafata baii,mai ales cand ea este continua. Acest fapt este folosit in practica de ex. in cazul turnarii alamelor in forme metalice, cand se face un adaos de aluminiu tocmai in vederea formarii peliculei de oxizi pentru a reduce evaporarea zincului, ai carui vapori se depun sub forma de ZnO pe peretii formei. Peliculele de acest gen in aliajele pe baza de cupru mai formeaza siliciul si beriliul;
- de presiunea de deasupra baii de metal. In vid temperatura de fierbere a metalelor se micsoreaza foarte mult. Acest lucru este utilizat uneori in practica pentru eliminarea unor impuritati din aliaje (distilarea in vid).
La topirea si supraincalzirea aliajelor, materialele metalice din incarcatura vin in contact cu atmosfera cuptorului, cu materialele de acoperire (zgure, fondanti) si cu captuseala cuptorului.
Intre cele trei faze care vin in contact (solida, lichida si gazoasa) au loc reactii chimice si fizico-chimice, care influenteaza atat randamentul in metal al elaborarii, cat si calitatea aliajului elaborat.
Principalele procese care au loc sunt de oxidare si de reducere, de dizolvare a gazelor si de difuziune a lor.
In atmosfera oxidanta metalele si aliajele neferoase, in comparatie cu cele feroase, au o comportare care prezinta unele particularitati:
cele mai multe metale neferoase au afinitate pentru oxigen mai mare decat fierul;
cele mai multe metale neferoase formeaza pelicule compacte de oxizi la suprafata baii;
la multe aliaje neferoase greutatea specifica a oxizilor este cu putin diferita fata de cea a aliajelor, ceea ce influenteaza mult procesul de dezoxidare.
Pentru determinarea afinitatii metalelor fata de oxigen se poate utiliza in scopuri practice valoarea caldurii de formare a oxizilor. Cu cat aceasta este mai mare, cu atat afinitatea pentru oxigen a metalului este mai mare.
Principalele metale care vin in considerare la elaborarea aliajelor neferoase pot fi astfel insiruite in ordinea cresterii afinitatii lor pentru oxigen:
![]()
tinand seama de caldura de formare a oxidului
Oxizii metalelor care se formeaza la elaborarea aliajelor
neferoase pot fi solizi, lichizi sau gazosi. Acesti oxizi (mai precis oxigenul)
pot fi dizolvati in aliajul lichid. (de ex. Cu![]() O in Cu, NiO in Ni, FeO in Fe, MnO in Mn) sau se pot gasi sub
forma de incluziuni nemetalice cu dimensiuni diferite (de ex. Al
O in Cu, NiO in Ni, FeO in Fe, MnO in Mn) sau se pot gasi sub
forma de incluziuni nemetalice cu dimensiuni diferite (de ex. Al![]() O
O![]() , SiO
, SiO![]() ,MgO, TiO
,MgO, TiO![]() si altii), care formeaza pelicule de oxizi la suprafata
baii.
si altii), care formeaza pelicule de oxizi la suprafata
baii.
In cazul dizolvarii metalelor si oxizilor lor in aliaje, afinitatea fata de oxigen se mareste odata cu cresterea activitatii concentratiei metalului in aliaj.
Aplicarea legii maselor arata ca in unele cazuri este posibila oxidarea in primul rand a metalului care are afinitate chimica mai mica pentru oxigen, insa concentratie mai mare. De exemplu, la elaborarea aliajului Cu - Al, in care Al este cu mult mai putin decat cuprul, se oxideaza concomitent ambele elemente, desi afinitatea aluminiului pentru oxigen este mult mai mare decat a cuprului.
In afara de afinitatea pentru oxigen si concentratia metalelor, oxidarea lor depinde de: timp, temperatura, suprafata baii, natura peliculei de oxizi, procesele de difuziune etc.
Cu marirea temperaturii oxidarea se intensifica, mai ales in cazul elementelor ai caror oxizi se dizolva in aliaje lichide (Cr, Ni).
Gradul si viteza de oxidare depinde si de caracterul, natura si proprietatile peliculelor (stratului) de oxizi care se formeaza la suprafata baii. Peliculele de oxizi pot fi:
stabile, continue si compacte. In acest caz, dupa formare, ele protejeaza baia de oxidare (ex. Al);
incompacte si poroase, care protejeaza slab baia de oxidare in timp ( Mg ).
Primul tip de pelicule se formeaza atunci cand raportul dintre volumul molecular al oxidului si volumul atomar al metalului este mai mare decat unitatea.
Peliculele de tipul doi se formeaza atunci cand acest raport este subunitar. In cazul principalelelor metale neferoase se intalnesc urmatoarele valori ale acestui raport ( la temperatura camerei):
![]() ;
; ![]() ;
; ![]() ;
; ![]() .
.
Rezulta ca metalele grele si aluminiul au raportul supraunitar, ceea ce indica formarea unei pelicule de oxid compact si continuu la suprafata baii. In acest caz viteza procesului de oxidare este determinata de viteza de difuziune a ionilor de metal spre exterior si a atomilor de oxigen spre interior (fig 10.2, curba aluminiului).
Pentru metalele Mg, Na, Ca raportul este subunitar, ceea ce denota formarea unui strat incompact si poros. Cand raportul este subunitar, oxidul format nu acopera integral suprafata metalului; oxigenul are acces direct la metale prin fisurile peliculei de oxizi.
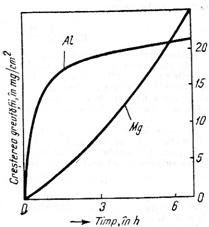
Fig 2
Variatia in timp a vitezei de oxidare (exprimata prin cresterea greutatii) a
aluminiului si magneziului la temperatura de
Fenomenul de oxidare nu este controlat de difuziune si relatia intre metalul oxidat si temperatura este o relatie liniara (fig.2 - curba magneziului)
Elementele care au afinitate mare pentru oxigen, pot schimba intr-o mare masura, chiar la continuturi mici, naura oxizilor metalului de baza. Astfel, in aliajele Al - Mg, in care magneziu este putin, pelicula de oxizi consta in principal din oxizi de magneziu este poroasa, incompacta, permite usor patrunderea oxigenului din atmosfera la suprafata aliajului si favorizeaza oxidarea baii.
Pe de alta parte, oxidarea aliajelor Al - Mg poate fi preintampianata prin adaosuri mici de beriliu, care are afinitatea pentru oxigen mai mare decat Al si Mg si formeaza o pelicula de oxizi mai compacta decat magneziul.
1 OXIDAREA METALELOR SI A ALIAJELOR NEFEROASE
Oxidarea aliajelor pe baza de cupru. Dintre componentii
cu caracter oxidant ai atmosferei cuprului, numai oxigenul liber si bioxidul de
sulf reprezinta medii oxidante pentru cupru, deoarece CO![]() si H
si H![]() O au tensiunea de disociere mai mica decat Cu
O au tensiunea de disociere mai mica decat Cu![]() O
O
In atmosfera ce contine oxigen liber, cuprul se oxideaza in stare solida, acoperindu-se treptat cu un strat de oxizi.
Daca atmosfera cuprului contine putin oxigen se formeaza
oxid cupros (Cu![]() O) care se dizolva in cuprul solid (v.fig.3).
O) care se dizolva in cuprul solid (v.fig.3).
Stratul de oxid cupros se formeaza incet si este aderent,
o parte din oxidul format(Cu![]() O) fiind consumat prin difuziune in masa de cupru.
O) fiind consumat prin difuziune in masa de cupru.
Daca atmosfera este foarte oxidanta se formeaza un strat gros de oxid cupric (CuO) mai bogat in oxigen, fie prin oxidarea directa a cuprului, fie prin reactia oxidului cupros:
[Cu]+1/2=(CuO)+ Q
[Cu![]() O]+1/2=2(CuO)+ Q
O]+1/2=2(CuO)+ Q
Oxidul cupric este insolubil in cuprul solid si stratul
de oxid se detasaza usor de masa cuprului. Acest fenomen este utilizat in
practica laminarii tablelor de cupru, cand lingoul, acoperit inca de la turnare
cu un strat de Cu![]() O, care patrunde prin difuzie in metal pe o adancime de
0,5.1,5 mm, este incalzit pentru laminare intr-o atmosfera puternic oxidanta,
ceea ce conduce la formarea CuO si la
detasarea acestuia de suprafata lingoului, care ramane neteda.
O, care patrunde prin difuzie in metal pe o adancime de
0,5.1,5 mm, este incalzit pentru laminare intr-o atmosfera puternic oxidanta,
ceea ce conduce la formarea CuO si la
detasarea acestuia de suprafata lingoului, care ramane neteda.
In cuprul lichid,oxidul cupros (Cu![]() O) ce se formeaza este solubil, ca FeO in aliajele de fier.
CuO nu se dizolva in cuprul lichid.
O) ce se formeaza este solubil, ca FeO in aliajele de fier.
CuO nu se dizolva in cuprul lichid.
In prezenta bioxidului de sulf din atmosfera cuptoarelor (rezultat prin arderea sulfului din pacura) are loc reactia:
6[Cu]+=[Cu![]() S] si 2[Cu
S] si 2[Cu![]() O]+ Q
O]+ Q
Cu![]() S si Cu
S si Cu![]() O se dizolva in cuprul lichid, iar la solidificare se separa
sub forma de eutectie fragil Cu - Cu
O se dizolva in cuprul lichid, iar la solidificare se separa
sub forma de eutectie fragil Cu - Cu![]() S si Cu - Cu
S si Cu - Cu![]() O la limita gruntilor (v. fig.3 a si b).
O la limita gruntilor (v. fig.3 a si b).
Asa cum sa aratat in cadrul oxizilor si sulfurilor care se dizolva in aliaj, solubilitatea este proportional cu radacina patrata a presiunii partiala a bioxidului de sulf si oxigenului din atmosfera.
Asadar, cuprul lichid si din aliaje, la temperaturile de
lucru cuprinse intre 1 000. 1 300 ![]() C se oxideaza in atmosfera cu oxigen si debioxid de sulf cu
formare de Cu
C se oxideaza in atmosfera cu oxigen si debioxid de sulf cu
formare de Cu![]() O si Cu
O si Cu![]() S.
S.
In cazul aliajelor de cupru care contin Al si Be (de ex.bronzuri cu Al si Be) procesul de oxidare este franat datorita formarii unei pelicule de oxizi care protejaza baia. Din acest motiv aceste bronzuri se pot topi, ca si aliajele de aluminiu, in atmosfera oxidanta.
Peliculele de oxizi de Mn si de Si au propietati intermediare.
Elementele din aliajele de cupru care au tensiunea de vapori ridicata (Zn si Mg) se oxideaza usor.Vaporii acestora se degaja in atmosfera oxidanta a cuptorului si se oxideaza, depunandu-se sub forma de particule solide pe suprafata baii sau sunt antrenate cu gazele.
Tendinta de oxidare a bronzurilor cu staniu este mai mica
decat a celorlalte bronzuri, totusi
datorita evaporarii zincului, pierderile prin oxidare pot fi mari, cu atat mai
mult cu cat capacitatea de protejare a peliculei de ZnO si Cu![]() O de la suprafata baii metalice este scazuta.
O de la suprafata baii metalice este scazuta.
Oxidarea
aliajelor pe baza de nichel. Deoarece NiO are tensiunea de disociere mai mica decat CO![]() ,H
,H![]() O si SO
O si SO![]() ,nichelul lichid la temperaturi ridicate de 1 500.1 700
,nichelul lichid la temperaturi ridicate de 1 500.1 700 ![]() C se oxideaza in prezenta tuturor componentilor din atmosfera
oxidanta, dupa reactiile:
C se oxideaza in prezenta tuturor componentilor din atmosfera
oxidanta, dupa reactiile:
[Ni]+1/2 ![]() [NiO]+ Q
[NiO]+ Q
[Ni]+ ![]() [NiO]+ - Q
[NiO]+ - Q
[Ni]+![]() [NiO]+2+ Q
[NiO]+2+ Q
7[Ni]+2![]() 4[NiO]+[Ni
4[NiO]+[Ni![]() S
S![]() ]+ Q
]+ Q
Reactiile sunt reversibile si se pot ajunge la echilibru cand concentratia gazelor produse ating valori determinate.
NiO si Ni![]() S
S![]() rezultate din reactii sunt solubile in nichelul lichid, dar
insolubile in nichelul solid in care se separa sub forma de eutectic la limita
grauntilor, ceea ce influienteaza negative proprietatile acestuia, intocmai ca
oxizi si sulfurile de cupru in cazului cuprului.
rezultate din reactii sunt solubile in nichelul lichid, dar
insolubile in nichelul solid in care se separa sub forma de eutectic la limita
grauntilor, ceea ce influienteaza negative proprietatile acestuia, intocmai ca
oxizi si sulfurile de cupru in cazului cuprului.
Hidrogenul rezultat in stare atomica se dizolva in aliaj desi atomsfera este oxidanta. Oxidul de carbon fiind isolubil in baie se indeparteaza, barbotand baia.
Oxidarea aliajelor pe baza de zinc, plumb si staniu. In atmosfera oxidanta toate aceste metale neferoase grele,usor fuzibili se oxideaza:
a)cu oxigenul: b)cu vaporii de apa:
[Zn]+1/2=(ZnO) [Zn]+=(ZnO)+2
[Pb]+1/2=(PbO) [Zn]+2=(SnO![]() )+4
)+4
[Sn]+ =(SnO![]() )
Pb nu se oxideaza in atmosfera de H
)
Pb nu se oxideaza in atmosfera de H![]() O
O
c) cu bioxidul de carbon d) cu bioxidul de sulf:
[Zn]+=(ZnO)+ 3[Zn]+ =2(ZnO)+(ZnS)
[Pb]+ =(PbO)+ 3[Pb]+ =(PbS)+2(PbO)
[Sn]+ =(SnO)+ 2[Sn]+
=(SnO![]() )+(SnS)
)+(SnS)
Produsele reactiilor (ZnO, PbO, SnO![]() , etc.) nu se dizolva in baia metalica.
, etc.) nu se dizolva in baia metalica.
Oxidarea aluminiului si a aliajelor lui are loc in toate gazele purtatoare de oxigen din atmosfera cuprului, cu exceptia oxidului de carbon, deoarece toate au tensiuni de disociere mai mari (caldura de formare mai mica):
4[Al] + 3=2(![]() ) 2[Al]+3=(
) 2[Al]+3=(![]() )+3
)+3
2[Al] +3=(![]() )+3 6[Al]+3=2(
)+3 6[Al]+3=2(![]() )+(
)+(![]() )
)
Oxidul format (![]() ) este insolubil in metalul de baza, atat in stare lichida
cat si in stare solida.
) este insolubil in metalul de baza, atat in stare lichida
cat si in stare solida.
Pelicula de ![]() , asa cum s-a arata, este continua, densa, compacta,
rezistenta, impermeabila si impiedica accesul oxigenului si a altor gaze oxidante
spre metalul de sub ea, incetinind oxidarea. Ca urmare, topirea si
supraincalzirea aluminiului si aproape a tuturor aliajelor pe baza de aluminiu
(cu exceptia celor din sistemul Al-Mg) pot fi efectuate in atmosfera oxidanta,
in conditiile nedistrugerii (prin amestecare) a peliculei de oxizi.
, asa cum s-a arata, este continua, densa, compacta,
rezistenta, impermeabila si impiedica accesul oxigenului si a altor gaze oxidante
spre metalul de sub ea, incetinind oxidarea. Ca urmare, topirea si
supraincalzirea aluminiului si aproape a tuturor aliajelor pe baza de aluminiu
(cu exceptia celor din sistemul Al-Mg) pot fi efectuate in atmosfera oxidanta,
in conditiile nedistrugerii (prin amestecare) a peliculei de oxizi.
![]() care rezulta din
oxidarea aluminiului cu
care rezulta din
oxidarea aluminiului cu ![]() este solid la
temperatura de topire a aluminiului si se indeparteaza in zgura.
este solid la
temperatura de topire a aluminiului si se indeparteaza in zgura.
Oxidarea aliajelor de magneziu are loc in contact cu toate gazele oxidante:
2[Mg]+=2(MgO)
4[Mg]+=2(MgO)+(![]() )
)
[Mg]+=(MgO)+ [Mg]+=(MgO)+[C]
2[Mg]+=2(MgO)+[C] 3[Mg]+=(MgO)+(
![]() )
)
[Mg]+=(MgO)+2
2[Mg]+=2(MgO)+[S]
3[Mg]+=2(MgO)+(MgS)
In cazul magneziului si al aliajelor de magneziu pelicula de oxizi de MgO (solid) care se formeaza la suprafata baii sau a metalului solid este poroasa, necompacta, deci permeabila pentru oxigen si gazele oxidante si nu protejeaza metalul contra oxidarii in continuare.
Cresterea in timp a greutatii piesei prin oxidare are loc liniar
Stratul de MgO fiind poros are o conductibilitate termica scazuta si joaca rol de izolator, impiedicand transmiterea in exterior a caldurii mari rezultate la oxidarea magneziului. In felul acesta temperatura sub stratul de oxid creste treptat si procesul de oxidare se accelereaza putandu-se ajunge si la evaporarea intensa si aprinderea vaporilor de magneziu. Rezulta ca topirea si supraincalzirea magneziului in atmosfera oxidanta nu se poate face decat sub strat protector de fondanti.
Pentru protejarea magneziului si a aliajelor lui contra oxidarii, in afara de fondanti se poate folosi microalierea cu beriliu (0,001.0,002%) care creaza o pelicula mult mai compacta la suprafata baii decat magneziul.
Beriliul se introduce fie sub forma de prealiaj Al-Be si
Al-Be-Mg sau sub forma de ![]() , din care beriliul se reduce si trece in solutie:
, din care beriliul se reduce si trece in solutie:
![]() +Mg=2NaF+Be+
+Mg=2NaF+Be+![]()
Oxidarea elementelor la topirea aliajelor se desfasoara in succesiunea corespunzatoare valorii tensiunii de disociere a oxizilor lor, in functie de concentratia lor si de tensiunile de vapori ale elementelor, atat in urma reactiei cu oxigenul, cat si in urma reactiei cu oxizii metalului de baza in care sunt solubili.
Asadar, oxidarea elementelor din aliaje are loc selectiv.
In cazul aliajelor lichide de cupru, solubilitatea ![]() in acestea este folosita la afanarea cuprului brut si a
deseurilor de calitate inferioara care contin 87.95% Cu, iar in rest: Zn, Fe,
Pb, Sn, As, S, Bi.
in acestea este folosita la afanarea cuprului brut si a
deseurilor de calitate inferioara care contin 87.95% Cu, iar in rest: Zn, Fe,
Pb, Sn, As, S, Bi.
Succesiunea de oxidare a elementelor (impuritatilor) obisnuite din aliajele pe baza de cupru este determinata de afinitatea elementelor pentru oxigen si anume:
![]() Al, Mg, Si, Zn, Fe, S, Sn, Pb,
As, Sb, Bi etc.
Al, Mg, Si, Zn, Fe, S, Sn, Pb,
As, Sb, Bi etc.
(de
ex. Zn+![]() =ZnO+2Cu; Pb+
=ZnO+2Cu; Pb+![]() =PbO+2Cu; 2As+3
=PbO+2Cu; 2As+3![]() =
=![]() +6Cu; Sb+2
+6Cu; Sb+2![]() =
=![]() +4Cu etc.).
+4Cu etc.).
DEZOXIDAREA ALIAJELOR NEFEROASE. RAFINAREA
Oxidarea, ca si evaporarea, care au loc in timpul elaborarii sunt procese nedorite.
Ele duc la pierderi de metal si la aparitia in aliaje a unor oxizi solubili sau insolubili care inrautatesc proprietatile mecanice si fizico-chimice ale acestora. In afara de acestea, prezenta oxizilor in alije poate determina aparitia sulfurilor in piese. La majoritatea aliajelor neferoase dezoxidarea se impune ca si in cazul aliajelor feroase.
La aliajele neferoase se utilizeaza doua mijloace de indepartare a oxigenului:
pe cale chimica (dezoxidare prin precipitare sau prin difuziune), in cazul cand oxidul este solubil (dizolvat) in metalul de baza lichid (de ex. la aliajele de cupru si de nichel);
pe cale fizica (prin barbotare, sedimentare sau dizolvare) in cazul in care oxidul este insolubil si se gaseste (nedizolvat) in metalul de baza lichid sub forma de suspensie sau emulsie (de ex. la aliajele pe baza de aluminiu si magneziu). Indepartarea oxizilor si deci a oxigenului prin antrenare (spalare) se numeste rafinare sau dezoxidare pe cale fizica.
Dezoxidarea pe cale chimica
Ca si in cazul aliajelor feroase, la dezoxidarea pe cale chimica se utilizeaza ca dezoxidant un element cu afinitate mai mare fata de oxigen decat metalul ce trebuie dezoxidat. Acest mod de dezoxidare se aplica la aliajele de cupru si de nichel, la care oxizii acestuia sunt dizolvati in baie metalica.
Dezoxidarea pe cale chimica poate fi:
prin precipitare, cand elementele dezoxidante se dizolva in baia metalica, iar oxizii lor insolubili se decanteaza in zgura;
prin difuziune, cand elementele dezoxidante nu se dizolva in baie metalica , iar oxigenul difuzeaza in baie metalica spre zgura.
La dezoxidarea prin precipitare elementele dezoxidante trebuie sa indeplineasca urmatoarele conditii:
sa aiba afinitate mai mare fata de oxigen decat metalul de baza;
sa fie solubile in metalul de baza astfel ca reactia chimica sa aiba loc cat mai avansat si in intreg volumul baii;
sa formeze oxizi care sa nu fie solubili in baia ce urmeaza a fi dezoxidata si sa se ridice usor la suprafata;
sa nu influenteze negativ proprietatile mecanice, fizice, chimice si de turnare ale aliajelor, tinand seama ca exista intotdeauna un exces de dezoxidant ramas in baie, necesar pentru dezoxidarea avansata;
sa aiba un pret de cost scazut si sa nu fie deficitare.
Dezoxidantii care pot fi utilizati la elaborarea aliajelor de cupru si de nichel, in functie de natura produselor de reactie, pot fi impartiti in trei grupe:
a) elemente care formeaza produse gazoase. Din aceasta grupa fac parte carbonul si gazele reducatoare, inclusiv hidrogenul si hidrocarburile. Carbonul ca dezoxidant se utilizeaza sub forma de prealiaj Ni-C in cazul aliajelor pe baza de nichel cand oxigenul este indepartat cub forma de CO.
Hidrogenul si oxidul de carbon reduc oxidul de cupru dand produse de reactie gazoase, insolubile in baie. Introducerea hidrogenului (operatie de persaj) in baia de cupru trebuie intrerupta in momentul cand oxidul cupros este redus in intregime. Dupa aceasta, barbotarea lui determina absortia si saturarea baii cu hidrogen.
Metoda se foloseste numai la dezoxidarea bailor de cupru, dupa perioada de oxidare, la obtinerea cuprului brut.
b)
elemente care formeaza produse
de dezoxidare sub forma de vapori sau lichide. Din aceasta grupa face parte
fosforul, utilizat la dezoxidarea aliajelor de cupru.Prin introducerea fosforului in cuprul oxidat, o
parte din el(cea care se gaseste la suprafata, in straturile superficiale ale
baii) reactioneaza cu oxidul cupros formand pentaoxidul de fosfor P![]() O
O![]() cu temperatura de topire 345
cu temperatura de topire 345![]() C si temperatura de fierbere 600
C si temperatura de fierbere 600![]() C:
C:
5[Cu![]() O]+2[P]=+10[Cu]+Q
O]+2[P]=+10[Cu]+Q
Vaporii de pentaoxid de fosfor au si un efect foarte favorabil de agitare a baii si de antrenare la suprafata a altor impuritati, ceea ce duce la marirea considerabila a fluiditatii aliajelor dezoxidate. Fosforul este in acelasi timp un dezoxidant si un fluidizant.
In volumul baii si partial la suprafata ei, fosforul
formeaza metafosfat de cupru (![]() ):
):
(![]() )+=2(
)+=2(![]() )
)
6(![]() )+2[P]=2(
)+2[P]=2(![]() )+10[Cu]
)+10[Cu]
Metafosfatul de cupru, la temperaturi de 1 000.1![]() , se gaseste in stare lichida, se ridica la suprafata baii
unde formeaza puncte de zgura fluide. Produsele de dezoxidare lichida au
avantajul ca iau forma sferica si se ridica usor la suprafata.
, se gaseste in stare lichida, se ridica la suprafata baii
unde formeaza puncte de zgura fluide. Produsele de dezoxidare lichida au
avantajul ca iau forma sferica si se ridica usor la suprafata.
In cazul aliajelor de cupru, produse de dezoxidare lichida se pot obtine si cu plumb:
[![]() ]+[Pb]=(PbO)+2[Cu]+Q
]+[Pb]=(PbO)+2[Cu]+Q
Oxidul de plumb are insa o greutate specifica ridicata
(7,8 g/![]() ) fata de cuprul lichid (8,4 g/
) fata de cuprul lichid (8,4 g/![]() ) si se separa greu si cu intarziere. In afara de aceasta,
plumbul, dupa cum s-a aratat, micsoreaza plasticitatea aliajelor de cupru si
deci nu poate fi utilizat ca dezoxidant.
) si se separa greu si cu intarziere. In afara de aceasta,
plumbul, dupa cum s-a aratat, micsoreaza plasticitatea aliajelor de cupru si
deci nu poate fi utilizat ca dezoxidant.
Produse lichide de dezoxidare se mai obtin in cazul folosirii litiului ca dezoxidant, atunci cand cuprul topit contine si oxigen si hidrogen (cand nu s-a stabilit echilibrul intre aceste 2 elemente):
2[![]() ]++2[Li]=2[Li(OH)]+4[Cu]+Q
]++2[Li]=2[Li(OH)]+4[Cu]+Q
Hidroxidul de litiu are temperatura de topire ![]()
Fosforul ca dezoxidant se foloseste sub forma de cupru fosforos eutectic, care este un prealiaj Cu-P cu 7.10% P.
Fosforul se introduce in cantitate de 0,005.0,03% (adica
0,15.0,3% prealiaj Cu-P cu 10% P). In cazul bronzurilor el mareste fluiditatea,
ceea ce usureaza turnarea. El mai formeaza pelicule de fosfati usor fuzibili de
tip 2ZnO![]() sau 3ZnO
sau 3ZnO![]() , mai fluide si mai elastice decat peliculele de ZnO, ceea ce
elimina posibilitatea impurificarii aliajelor cu ZnO.
, mai fluide si mai elastice decat peliculele de ZnO, ceea ce
elimina posibilitatea impurificarii aliajelor cu ZnO.
c) elemente care formeaza produse solide de dezoxidare, insolubile in metal, care au capacitatea sa treaca partial sau total in zgura. La aliajele pe baza de cupru si de nichel, majoritatea elementelor neferoase formeaza oxizi insolubili (de ex.: Al, Zn, Mn, Si, etc.).
Desi au capacitate mare de dezoxidare, elementele aratate nu se utilizeaza ca dezoxidanti deoarece produsele de dezoxidare (oxizii lor) se indeparteaza greu din baie, ca urmare a umectibilitatii lor ridicate.
Piesele turnate din aliaje dezoxidate cu aceste elemente au proprietati mecanice scazute.
Pentru obtinerea unor produse de dezoxidare usor de indepartat, in practica se folosesc dezoxidanti complecsi, care constau din unul sau mai multe elemente cu afinitate mare pentru oxigen.
Elementele care intra in compozitia acestor dezoxidanti permit realizarea unor compusi complecsi in stare lichida, care se indeparteaza usor din baie. In afara de aceasta, prezenta in dezoxidant a mai multor elemente active, insa in proportii mici, micsoreaza pericolul impurificarii excesive a aliajului cu unul din aceste elemente.
Se pot da urmatoarele exemple de dezoxidanti complecsi:
pentru obtinerea cuprului pur (pentru scopuri electrotehnice) amestecul de
borax (![]() ) cu praf de magneziu in raport de greutate 95:5. Elementele
dezoxidante sunt Mg si B. Produsele de dezoxidare (MgO, in general greu de
indepartat) se indeparteaza concomitent cu picaturile de fondant;
) cu praf de magneziu in raport de greutate 95:5. Elementele
dezoxidante sunt Mg si B. Produsele de dezoxidare (MgO, in general greu de
indepartat) se indeparteaza concomitent cu picaturile de fondant;
pentru aliajele de nichel se utilizeaza prealiaje de Ni-Mn-Mg, care indeparteaza si sulful.
Cate odata, cand se urmareste dezoxidarea avansata, se utilizeaza si dezoxidanti ai caror oxizi se indeparteaza greu din baie (de ex. Mg in cazul aliajelor de Cu).
Un dezoxidant puternic pentru aliajele de cupru si de nichel este litiul:
[![]() ]+2Li=
]+2Li=![]() +2[Cu]+Q
+2[Cu]+Q
[NiO]+2Li=![]() +[Ni]+Q
+[Ni]+Q
Oxidul de litiu solid (![]() ) este insolubil in aliajul lichid.
) este insolubil in aliajul lichid.
Dezoxidarea prin difuziune se aplica atunci cand se urmareste eliminarea oxigenului din baie, fara dizolvarea elementelor dezoxidante, deci cand se urmareste obtinerea unor aliaje de puritate ridicata.
In aceste conditii aliajul dezoxidat este complet lipsit atat de dezoxidant in exces, cat si de suspensiile de oxizi ai acestuia.
In cazul dezoxidarii cu precipitare, anumite proportii de elemente dezoxidante (P, C) sau de oxizi (MgO, MnO) raman in aliaje si oricat de mici ar fi, influenteaza negativ unele proprietati (de ex. conductibilitatea electrica la cupru).
La dezoxidarea prin difuziune a cuprului, substantele dezoxidante se presara sub forma de pulberi la suprafata baii de cupru unde are loc o micsorare a concentratiei de oxigen. In felul acesta se creaza un gradient de concentratie al oxigenului, care face ca acesta din urma sa difuzeze din straturile adanci spre suprafata baii metalice.
Metoda are avantajul ca aliajul dezoxidat de obtine mai pur. Dezavanajul ei e durata mai mare a procesului de dezoxidare.
Dezoxidantii utilizati in acest scop se numesc dezoxidanti de suprafata spre deosebire de dezoxidantii de adancime folositi la dezoxidarea prin precipitare.
Dezoxidantii de suprafata care se folosesc mai frecvent
in cazul cuprului sunt urmatorii: carbura de calciu (![]() ); borura de magneziu (
); borura de magneziu (![]() ); carbonul (mangalul) si azura borica. Aceasta din urma se
obtine din reactia boraxului (
); carbonul (mangalul) si azura borica. Aceasta din urma se
obtine din reactia boraxului (![]() ) cu praful de magneziu din amestecul in raport de greutate
(95:5) care se presara pe suprafata baii sau din reactia anhidridei borice cu
magneziul:
) cu praful de magneziu din amestecul in raport de greutate
(95:5) care se presara pe suprafata baii sau din reactia anhidridei borice cu
magneziul:
(![]() )+[Mg]=(
)+[Mg]=( ![]() ) sau
) sau
(![]() )+[Mg]=(
)+[Mg]=( ![]() )
)
Reactiile de dezoxidare care au loc sunt:
5[![]() ]+(
]+(![]() )=(CaO)+2+10[Cu]+Q
)=(CaO)+2+10[Cu]+Q
6[![]() ]+(
]+(![]() )=3(MgO)+(
)=3(MgO)+( ![]() )+12[Cu]
)+12[Cu]
2[![]() ]+[C]=+4[Cu]+Q
]+[C]=+4[Cu]+Q
[![]() ]+(
]+(![]() )=(
)=( )+2[Cu]
)+2[Cu]
Dezoxidantul este oxidul inferior al borului![]() care se oxideaza la
care se oxideaza la ![]() cu oxidul din baie.
Zgura borica fiind o sare nu se dizolva in cuprul topit.
cu oxidul din baie.
Zgura borica fiind o sare nu se dizolva in cuprul topit.
Primii trei dezoxidanti se adauga si raman la suprafata in stare de pulbere, in timp ce zgura borica si produsele de dezoxidare obtinute cu aceasta sunt lichide la temperatura cuprului topit. Durata de dezoxidare se poate scurta prin amestecarea zgurei borice in metalul lichid.
Dupa cum se vede, elementele dezoxidante la dezoxidare
prin difuziune sunt carbonul si suboxidul de bor (![]() ).
).
Dezoxidarea cu dezoxidanti de suprafata este cu totul analoaga dezoxidarii prin difuziune a otelurilor la elaborarea lor in cuptoare electrice cu arc, cu zgura alba sau carbidica (dezoxidarea cu carbon).
Asadar principalii dezoxidanti folositi pentru cupru, nichel si aliajele lor sunt:
Pentru cupru si aliaje de cupru:
Dezintoxicare prin precipitare
- cupru fosforos (cu 7.8% P sau 10% P);
- litiu, prealiaj Cu-Li (cu 1% Li);
- prealiaj Cu-Si;
- prealiaj Si-Mn;
- prealiaj Cu-Be;
- Dezintoxicare prin difuzie
- carbidul (![]() );
);
- borura de magneziu (![]() );
);
- suboxidul de bor (![]() ) din zgura borica;
) din zgura borica;
- carbonul (mangalul);
Pentru nichel si aliaje de nichel:
- Dezintoxicare prin precipitare
- litiu si prealiaj Cu-Li (1% Li);
- prealiaj Al-Ni;
- prealiaj Mg-Zn;
- prealiaj Mg-Cu;
- prealiaj complex Mn-Al-C;
- prealiaj complex Mg-Mn-Si.
La aliajele de nichel se foloseste mai putin dezoxidarea prin difuziune.
Dezoxidarea pe cale fizica
Dezoxidarea pe cale fizica reprezinta indepartarea prin antrenare a oxizilor insolubili, care se gasesc in suspensie in metalul lichid de baza. Se mai numeste si rafinare pentru ca in timpul dezoxidarii, pe langa incluziuni, se indeparteaza partial si gazele.
Acest procedeu de dezoxidare se aplica la majoritatea aliajelor neferoase si mai ales la cele de aluminiu, de magneziu si la aliajele de cupru care contin aluminiu.
Utilizarea dezoxidarii pe cale chimica in cazul cand oxizii sunt insolubili este imposibila din doua motive:
pentru unele aliaje (de ex. cele de aluminiu si de magneziu) se gasesc cu greu metale care sa aiba afinitate fata de oxigen sensibil mai mare decat metalele de baza;
oxizii nefiind dizolvati in metalul lichid nu pot fi pusi in contact intim cu un dezoxidant solubil in baie.
In majoritatea cazurilor (cu unele exceptii), oxizii metalelor au greutatea spacifica mai mica decat a metalului lichid si de aceea pot decanta (sedimenta) la suprafata.
Viteza de decantare a incluziunilor oxidice este cu atat mai mare cu cat:
diferenta de greutate specifica dintre oxid si metal este mai mare;
dimensiunile lor sunt mai mari;
forma lor este mai rotunda;
umectarea lor de catre metalul lichid este mai slaba.
La aliajele de aluminiu si de magneziu, oxizii nu numai ca sunt insolubili, dar se gasesc in suspensie sub forma de pelicule ramificate cu dimensiuni foarte mici (sutimi sau miimi de milimetru).
Dimensiuni mici au in special produsele de dezoxidare prin precipitare, insolubile in metalul lichid, deoarece acestea se gasesc fin dispersate in toata masa lui.
Greutatea specifica a aluminei compacte (![]() ) variaza intre 3,55 si 4,15 g/
) variaza intre 3,55 si 4,15 g/![]() , in functie de starea alotropica, iar cea a aluminiului
topit intre 2,3 si 2,4 g/
, in functie de starea alotropica, iar cea a aluminiului
topit intre 2,3 si 2,4 g/ ![]() . In realitate, alumina formata la elaborare are un numar
mare de pori umpluti cu gaze, ceea ce face ca greutatea specifica a ei sa fie,
dupa imprejurari, ceva mai mare, egala sau chiar mai mica decat a aluminiului.
. In realitate, alumina formata la elaborare are un numar
mare de pori umpluti cu gaze, ceea ce face ca greutatea specifica a ei sa fie,
dupa imprejurari, ceva mai mare, egala sau chiar mai mica decat a aluminiului.
De asemenea, greutatea specifica a oxidului de magneziu este cu putin mai mica decat a magneziului topit.
Indepartarea acestor oxizi prin sedimentare are loc cu o viteza foarte mica , chiar si in cazul cand greutatea specifica a aliajului este cu mult mai mare decat a oxidului (de ex. bronzul cu aluminiul).
In scopul maririi diferentei dintre greutatea specifica a oxizilor (de Al, Mg) si metalul lichid nu poate fi utilizata nici cresterea temperaturii acestuia, deoarece se intensifica tendinta de absortie a gazelor (si mai ales a hidrogenului).
Indepartarea oxizilor insolubili, deci dezoxidarea pe cale fizica (rafinarea) se poate realiza la randul ei in doua moduri:
prin antrenare cu gaze (spalare sau flotare);
prin antrenare cu fondanti.
a. Indepartarea oxizilor insolubili cu ajutorul gazelor , consta in crearea a numeroase bule de gaze sau de vapori in intreaga masa de aliaj lichid, care ridicandu-se spre suprafata antreneaza oxizii solizi.
Pentru a fi antrenate, particulele de oxizi trebuie sa piarda umectibilitatea cu metalul. Cand bulele se distrug la suprafata baii, particulele de oxizi , ramanad neumectate, se mentin la acest nivel, de unde sunt apoi indepartate sub forma de zgura.
Bulele de gaze pot fi create prin introducerea in baie (barbotare) a gazelor inerte (azot, argon). Durata de suflare este de 8.15 min., iar consumul de 0,3.1,0% din greutatea metalului lichid (fig. 3, a).
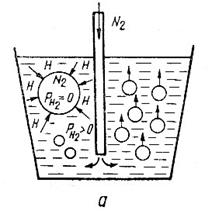

Fig. 10.3 Modul de antrenare a oxizilor si gazelor de catre bulele de gaze in cazul folosirii azotului (a) si a clorurlui (b) pentru rafinare
In cazul aliajelor de aluminiu se pot produce bule de
vapori de clorura de aluminiu (![]() ), care au punctul de fierbere
), care au punctul de fierbere ![]() si care la temperatura
de elaborare a acestor aliaje (690.
si care la temperatura
de elaborare a acestor aliaje (690.![]() ) se gasesc in stare de vapori.
) se gasesc in stare de vapori. ![]() are aproximativ
aceeasi capacitate de rafinare ca si gazul inert (fig. 3, b).
are aproximativ
aceeasi capacitate de rafinare ca si gazul inert (fig. 3, b).
In acest scop in baia de aluminiu se introduc urmatoarele cloruri (saruri) cu ajutorul
cutiilor sau clopotelor cu orificii sau sub forma de brichete cu greutate spacifica scazuta (![]() ):
):
Sarea Temperatura de Temperatura de
topire, in ![]() fierbere, in
fierbere, in ![]()
![]() 318 732
318 732
![]() 650 1 190
650 1 190
![]() 193 182
193 182
In acelasi scop se folosesc ![]() si
si ![]() .
.
Reactia descopunerii sarurilor are loc dupa urmatoarea schema:
3
MeClm+m Al ![]() mAlCl
mAlCl![]() +3 Me
+3 Me
3
ZnCl![]() +2 Al=2 AlCl
+2 Al=2 AlCl![]() +3 Zn
+3 Zn
3
MnCl![]() +2 Al=2 AlCl
+2 Al=2 AlCl![]() +3 Mn
+3 Mn
Metalul redus din sare trece in aliaj si poate avea influente diferite.
De ex. manganul rezultat din ![]() creeaza in aliaj
germeni suplimentari de cristalizare, finiseaza structura si imbunatateste
proprietatile mecanice. Zincul rezultat din
creeaza in aliaj
germeni suplimentari de cristalizare, finiseaza structura si imbunatateste
proprietatile mecanice. Zincul rezultat din ![]() micsoreaza
proprietatile mecanice si de coroziune.
micsoreaza
proprietatile mecanice si de coroziune.
Parametrii principali ai operatiei de tratare cu saruri sunt urmatorii:
consumul de saruri este de 0,05 pana la 0,2.0,5% (este cu atat mai mare cu cat cantitatea de impuritati -oxizi este mai ridicata, depinzand si de capacitatea de rafinare a sarii);
cantitatile mari de saruri se introduc in mai multe etape (doua-trei);
durata de prelucrare a baii cu saruri trebuie sa fie indelungata (3.5
min.). Reactia de producere a vaporilor sa aiba loc incet pentru a putea creea
conditii bune de contact dintre bulele de vapori si oxizi. Rezulta ca bulele de
vapori trebuie sa fie mici. Dintre saruri, ![]() este cea mai eficace,
deoarece are temperatura de fierbere cea mai mare;
este cea mai eficace,
deoarece are temperatura de fierbere cea mai mare;
turnarea aliajului de face dupa 5.15 min. dupa rafinare pentru a asigura conditii prielnice de indepartare a oxizilor;
pastrarea sarurilor trebuie sa se faca in locuri fara umezeala, deoarece
ele sunt higroscopice (mai ales ![]() ). Introducerea clorurii umede in baia de aluminiu, provoaca
degajari bruste de hidrogen si ca urmare aruncari si proiectari in exterior de
metal lichid (explozii):
). Introducerea clorurii umede in baia de aluminiu, provoaca
degajari bruste de hidrogen si ca urmare aruncari si proiectari in exterior de
metal lichid (explozii):
2[Al]+3 (din clorura umeda)=( ![]() )+6+Q
)+6+Q
In baie creste proportia de ![]() si de hidrogen, desi
se urmareste prin rafinare micsorarea continutului lor;
si de hidrogen, desi
se urmareste prin rafinare micsorarea continutului lor;
tratarea cu saruri se realizeaza mai bine in cuptoare cu capacitate mica si mijlocie, cu baie adanca;
folosirea hexacloretanului (![]() ) prezinta avantajul ca acesta nu este higroscopic si creeaza
vapori suplimentari de tetracloretilen (
) prezinta avantajul ca acesta nu este higroscopic si creeaza
vapori suplimentari de tetracloretilen (![]() ):
):
3 ![]() =3
=3![]() +3
+3![]()
2 Al+3![]() =2
=2![]()
3(![]() )+2[Al]=3+2
)+2[Al]=3+2
Tetracloretilenul rezultat (![]() ) este lichid la temperatura camerei si are temperatura de
fierbere
) este lichid la temperatura camerei si are temperatura de
fierbere ![]() Transformandu-se in
vapori, el actioneaza concomitent cu vaporii de
Transformandu-se in
vapori, el actioneaza concomitent cu vaporii de ![]() . Aproximativ 30% din
. Aproximativ 30% din ![]() intra in reactia cu
aluminiul.
intra in reactia cu
aluminiul.
Rafinarea cu saruri de clor se utilizeaza si in cazul bronzurilor cu aluminiu si al aliajelor Al-Mg, al aliajelor pe baza de plumb, staniu si de zinc, la care oxizii sunt insolubili in aliajul de baza lichid.
Astfel, la aliajele Al-Mg, clorul reactioneaza atat cu aluminiul cat si cu magneziul:
[Mg]+=(![]() )+Q
)+Q
3[Mg]+2=2[Al]+3(![]() )+Q
)+Q
La temperatura 700.710![]() C se formeaza in principal
C se formeaza in principal ![]() iar la temperatura de
740.750
iar la temperatura de
740.750![]() C - mai mult
C - mai mult ![]() , ceea ce determina micsorare continutului de magneziu, ce
trebuie compensat. Rezulta ca la aliajele Al-Mg temperatura baii la
introducerea sarurilor de clor trebuie sa fie cuprinsa intre 700 si 730
, ceea ce determina micsorare continutului de magneziu, ce
trebuie compensat. Rezulta ca la aliajele Al-Mg temperatura baii la
introducerea sarurilor de clor trebuie sa fie cuprinsa intre 700 si 730![]() C pentru a evita pierderile de magneziu.
C pentru a evita pierderile de magneziu.
De asemenea la aliajele Al-Mg si Al-Si se pot utiliza
pentru rafinare fluorurile, ca de exemplu: fluorzirconatul de potasiu (![]() ) sau fluorzirconatul de sodiu (
) sau fluorzirconatul de sodiu (![]() ) in proportie de 0,5.1%:
) in proportie de 0,5.1%:
3![]() +4Al=4Al
+4Al=4Al![]() +6KF+3Zr
+6KF+3Zr
![]() sub forma de vapori
antreneaza oxizii si gazele , iar zirconiul formeaza probabil cu hidrogenul
compusul ZrH si prin aceasta ii micsoreaza continutul in aliaje.
sub forma de vapori
antreneaza oxizii si gazele , iar zirconiul formeaza probabil cu hidrogenul
compusul ZrH si prin aceasta ii micsoreaza continutul in aliaje.
La aliajele de Pb, Zn si Sn se utilizeaza mai mult pentru
rafinare clorura de amoniu care sublimeaza la ![]() , vaporii antrenand cu ei oxizii in suspensie.
, vaporii antrenand cu ei oxizii in suspensie.
b. Indepartarea oxizilor insolubili cu ajutorul fondantilor. Rafinarea in acest caz consta in colectarea peliculelor solide de oxizi de catre particulele lichide de fondant din baia metalica.
Efectul de rafinare se bazeaza pe fenomenele care au la suprafata metal-oxid-fondant lichid (deci o faza solida si doua lichide).
Particulele (peliculele) solide de oxizi trec in fondant si pot fi colectate (zgurificate) cand se realizeaza urmatoarele conditii:
![]()
![]()
unde:
![]() sunt tensiunile
interfaciale la suprafata metal-lichid, oxid-solid (M-O). fondant lichid-metal
lichid (F-M), fondant lichid-oxid solid (F-O).
sunt tensiunile
interfaciale la suprafata metal-lichid, oxid-solid (M-O). fondant lichid-metal
lichid (F-M), fondant lichid-oxid solid (F-O).
Tensiunea superficiala poate fi exprimata prin unghiul de umectare (fig. 4).

Fig. 4. Conditiile de indepartate a oxizilor de aluminiu cu ajutorul fondantilor si procesul de zgurificare: a- fondantul lichid F umecteaza incluziunea solida Al2O3; unghiul θ este mic; b - aliajul lichid M nu umecteaza incluziunea solida Al2O3; unghiul θ este mare; c - fondantul lichid F umecteaza partial aliajul lichid M; d - modul de antrenare a incluziunii Al2O3 de catre particula de fondant lichid
Cu cat tensiunea superficiala la suprafata fondant-oxid (![]() ) este mai mica, cu atat fondantul il umecteaza mai bine pe
acesta din urma (il infasoara) si il separa (izoleaza) de metalul lichid.
) este mai mica, cu atat fondantul il umecteaza mai bine pe
acesta din urma (il infasoara) si il separa (izoleaza) de metalul lichid.
Cu cat este mai mare tensiunea superficiala la suprafata
fondant-metal (![]() ) cu atat primul se poate separa mai usor de metalul lichid.
De asemenea, cu cat este mai mare tensiunea superficiala metal-oxid (
) cu atat primul se poate separa mai usor de metalul lichid.
De asemenea, cu cat este mai mare tensiunea superficiala metal-oxid (![]() ), cu atat ultimul poate fi indepartat mai usor.
), cu atat ultimul poate fi indepartat mai usor.
Cu alte cuvinte, pentru realizarea dezoxidarii cu fondant, acesta trebuie sa se gaseasca in baia metalica in stare lichida, sa infasoare particulele solide de oxizi (deci, sa le umecteze bine) si apoi intr-un timp scurt sa se ridice impreuna cu ele la suprafata (sau sa se coboare), adica sa fie umectate cat mai putin de metalul lichid.
In felul acesta, la suprafta baii se aduna fondantul cu oxizi sub forma de zgura lichida.
Asadar, mecanismul de baza al indepartarii oxizilor consta in capacitatea de absortie a acestora de catre fondant.
Partial poate avea loc si un proces de dizolvare a oxizilor in fondant.
Pentru accelerarea procesului de dezoxidare se imbunatateste contactul dintre particulele lichide de fondant si oxizi prin amestecarea baii.
Compozitia fondantului joaca rolul hotarator. Din acest motiv, fondantii dezoxidanti trebuie sa aiba urmatoarele proprietati:
temperatura de topire mai joasa decat a metalului sau a aliajului;
fluiditate buna, adica capacitate mare de absortie;
tensiune superficiala mare la suprafata de contact cu metalul lichid pentru a forma o pelicula compacta la suprafata baii (rol protector) si pentru a se separa usor din metal (rol absorbant);
vascozitate suficienta la temperatura de turnare a metalului, pentru a se separa usor si de a nu fi antrenat de aceasta in forma.
Rafinarea cu fondanti se aplica pe scara larga la aliajele de magneziu, la care oxizii se gasesc in suspensie si au greutatea specifica foarte apropiata de cea a metalului.
In functie de temperatura de supraincalziere, metalul poate fi mai greu, mai usor sau sa aiba practic aceeasi greutate ca oxizii lui (fig. 5).

Fig 5. Variatia greutatii specifice a metalului γm si a oxizilor sai γ0 in functie de temperatura t de supraincalzire in stare lichida
In cazul cand oxizii in suspensie sunt mai usori (temperatura de supraincalzire a metalului relativ mica) ei se concentreaza in partea superioara a baii.
Fondantul utilizat trebuie sa fie si el mai usor decat metalul (fondant de suprafata, fondant usor). Dupa presararea lui pe suprafata baii sau dupa introducerea lui sub forma de pulbere la fundul baii, el se topeste si particulele lichide de fondant se ridica la suprafata, colectand dupa mecanismul aratat, peliculele mici de oxizi. Prin purificarea metalului are loc cresterea greutatii lui specifice, ceea ce face ca straturile superioare de metal sa se deplaseze in jos, locul lor fiind ocupat de un alt strat bogat in oxizi, mai usor, creandu-se astfel un curent de convectie, care favorizeaza indepartarea oxizilor (fig. 6, a).
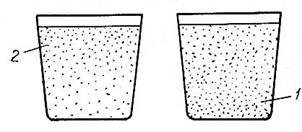

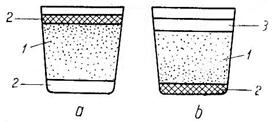
Fig 6. Modul de repartizare a oxizilor si fondantilor in aliaje de magneziu in cazul cand fondantul este mai usor (a) si mai greu (b) decat aliajul lichid: 1 - oxizi in baia de metal; 2- strat de fondant + oxizi; 3 - strat de metal purificat.
In cazul in care oxizii sunt mai grei decat metalul (temperatura de supraincalzire mare), acestia se concentreaza (sedimenteaza) in partile inferioare ale baii (spre vatra). Fondantul folosit pentru rafinare trebuie sa aiba si el o greutate spacifica mai mare decat metalul (fondant de adancime, fondant greu). La introducerea lui in metal (la suprafata sau in interior cand se amesteca cu metalul), el se topeste si sub forma de particule lichide strabate coloana de metal de sus in jos, colectand oxizii in suspensie. Fondantul impreuna cu oxizii se depune pe vatra.
In contact cu stratul de fondant de pe vatra, portiunile de metal se purifica, isi micsoreaza greutatea specifica (oxizii fiind mai grei) si se ridica spre suprafata. Astfel, se realizeaza si de aceasta data un curent de convectie, care favorizeaza afinarea (fig. 6, b).
Cand oxizii au greutate specifica aproximativ egala cu cea a metalului si sunt raspanditi practic in tot volumul baii, se utilizeaza pentru dezoxidare fie fondanti grei (de adancime), fie fondanti usori (de suprafata), care in drum spre vatra sau spre suprafata colecteaza impuritatile.
Acesta ar fi cazul cel mai favorabil, deoarece implica o supraincalzire normala a aliajelor de magneziu si aluminiu.
In practica insa se utilizeaza mai mult fondanti grei, intrucat cu greu se pot produce fondanti mai usori decat aliajele (de ex. cele de magneziu).
c. Dezoxidarea prin filtrare. Oxizii de Al, Ti, Zr si Be, care nu se dizolva in aliajul lichid pot fi retinuti prin filtrare.
Filtarea poate fi de mai multe tipuri:
mecanica, in care caz se folosesc site metalice sau din sticla refractara,
prin care trece aliajul la evacuarea acestuia din cuptor. Reteaua sitei este de
0,5![]() 0,5 mm (la aliajele de aluminiu);
0,5 mm (la aliajele de aluminiu);
fizico-chimica, in care caz filtrarea se realizeaza printr-un strat de
granule de ![]() si
si ![]() sau din alte materiale
imbibate cu saruri active. Acest procedeu de filtrare asigura in comparatie cu
precedentul, continuturi de incluziuni de 2.10 ori mai mici si de gaze cu
30.40% mai scazute;
sau din alte materiale
imbibate cu saruri active. Acest procedeu de filtrare asigura in comparatie cu
precedentul, continuturi de incluziuni de 2.10 ori mai mici si de gaze cu
30.40% mai scazute;
chimica , in care caz se practica trecerea jetului de aliaj printr-un strat de saruri lichide active.
La filtrarea fizico-chimica se realizeaza absortia incluziunilor de catre sarurile din filtru.
Procedeele se aplica la aliajele de aluminiu, magneziu, zinc.
|
Politica de confidentialitate |
| Copyright ©
2025 - Toate drepturile rezervate. Toate documentele au caracter informativ cu scop educational. |
Personaje din literatura |
| Baltagul caracterizarea personajelor |
| Caracterizare Alexandru Lapusneanul |
| Caracterizarea lui Gavilescu |
| Caracterizarea personajelor negative din basmul |
Tehnica si mecanica |
| Cuplaje - definitii. notatii. exemple. repere istorice. |
| Actionare macara |
| Reprezentarea si cotarea filetelor |
Geografie |
| Turismul pe terra |
| Vulcanii Și mediul |
| Padurile pe terra si industrializarea lemnului |
| Termeni si conditii |
| Contact |
| Creeaza si tu |